So sánh công nghệ giải trình tự Pyrosequencing và Sanger Sequencing
Sanger sequening và Pyrosequencing là hai phương pháp giải trình tự phổ biến hiện nay với những ứng dụng khác nhau. Khác với giải trình tự thế hệ mới NGS, các thiết bị sử dụng công nghệ Pyrosequencing và Sanger Sequencing đều là những thiết bị công suất từ nhỏ đến trung bình với chi phí hợp lý đang được sử dụng khá phổ cho nghiên cứu và chuẩn đoán tại Việt Nam. Mỗi công nghệ và thiết bị có những ứng dụng thế mạnh riêng, tuỳ vào mục đích ứng dụng không chỉ loại trừ nhau, mà còn bổ sung cho nhau. Bài viết nhằm cung cấp kiến thức tổng quan cho những nhà nghiên cứu, ứng dụng có thêm thông tin lựa chọn khi đầu tư thiết bị giải trình tự không phải NGS.
So sánh công nghệ giải trình tự Pyrosequencing và Sanger Sequencing
1. Phương pháp Sanger Sequencing
Phương pháp Sanger Sequencing hay còn gọi là phương pháp enzyme được Sanger và cộng sự phát minh năm 1977.
Hiện nay phương pháp này được cải tiến để tiến hành phản ứng trong 1 ống nghiệm và sử dụng phương pháp điện di mao quản. Điểm chính của phương pháp này được tóm tắt như sau:
+ Trong ống phản ứng chứa 1 primer, sợi khuôn, emzyme DNA Polymerase, 4 loại nu dNTP và số lượng có hạn các ddNTP: ddATP, ddGTP, ddCTP và ddTTP (dNTP loại gốc -OH tại vị trí 3' của đường deoxyribo). các ddNTP được đánh dấu bằng 4 màu huỳnh quang khác nhau.
+ Khi DNA Polymerase kéo dài mạch các dNTP và cả ddNTP sẽ được thêm vào mạch mới, việc gắn ddNTPhay dNTP vào mạch là ngẫu nhiên, do đó sau mỗi chu kỳ sẽ có đồng thời cả mạch chứa dNTP (A, T, G, C) và ddNTP (A, T, G, C).
+ Các đoạn được gắn ddNTP vào sẽ dừng lại không thể làm khuôn cho chu kỳ tổng hợp tiếp theo; các sợi được gắn dNTP sẽ tiếp tục đi vào chu kỳ tiếp theo và được gắn thêm Nucleotide mới và tạo thành các sản phẩm hơn kém nhau 1 Nucleotide. Phản ứng giải trình tự tiến hành 30-40 chu kỳ PCR
+ Sản phẩm sẽ được điện di trên mao quản để phân biệt các sản phẩm hơn kém nhau 1 nucleotide tương ứng ứng với trình tự của đoạn DNA. Do vậy phương pháp này còn gọi được gọi là DNA Sequencing by Capillary Electrophoresis
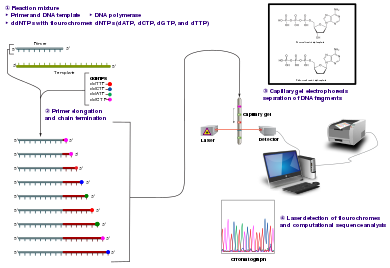
Chi tiết tham khảo thêm http://www.vsmmb.com/data/upload_file/File/PCR%20book%201/PCR_sequencing.pdf
2. Tổng quan về phương pháp Pyrosequencing
Công nghệ pyrosequencing dựa trên cơ sở pyrophosphate (PPi) được giải phóng khi nucleotide tự do mới được gắn vào chuỗi trong quá trình tổng hợp sợi DNA. Sau mỗi nucleotide tự do được gắn vào sợi khuôn trong quá trình tổng hợp, PPi giải phóng được phát hiện nhờ phức hợp enzyme chuyển thành tín hiệu quang học và được phát hiện bởi một CCD cực nhạy.
Công nghệ Pyrosequencing cũng là 1 loại giải trình tự bởi quá trình sinh tổng hợp (Sequencing by Synthesis - SBS) hay còn gọi là Real-time Sequencing Nguyên lý gồm các bước sau:
Bước 1: Một đoạn DNA được khuếch đại và sợi làm bản mẫu cho pyrosequencing được biotin hoá. Sau khi biến tính, sợi đơn PCR amplicon được phân lập và được lại với một primer giải trình tự.
Bước 2: Phức hợp lai của primer và sợi đơn khuôn được ủ với phức hợp men (enzyme) DNA polymerase, ATP sulfurylase, luciferase, and apyrase và các cơ chất adenosine 5 'phosphosulfate (APS) và luciferin

Bước 3: Deoxyribonucleotide triphosphate (dNTP) đầu tiên được thêm vào phản ứng. DNA polymerase xúc tác gắn thêm dNPT vào primer giải trình tự, nếu nó bổ sung với trình tự sợi khuôn. Mỗi một sự kiện gắn vào đó đi kèm với việc giải phóng pyrophosphate (PPi). Số phân tỷ PPi giải phóng bằng với số nucleotide được gắn vào.

Bước 4: ATP sulfurylase biến đổi PPi thành ATP với sự hiện diện của APS. Phân tử ATP này điều khiển việc chuyển hoá luciferin thành oxiyluciferin dưới sự xúc tác của luciferase tạo ra ánh sáng khả kiến tỷ lệ thuận với số phân tử ATP. Ánh sáng được tạo ra trong phản ứng luciferase xúc tác được phát hiện bởi các cảm biến CCD (CCD senser) và được nhìn thấy thành các đỉnh trong dữ liệu đầu ra thô (Pyrogram®). Độ cao của mỗi đỉnh (light signal) tỷ lệ thuận với nu được gắn vào

Bước 5: Apyrase liên tục phân giải nucleotide (dNTP) không được gắn vào (không bổ với mạch khuôn) và các ATP sinh ra. Khi quá trình phân giải hoàn thành, một nucleotide khác được thêm vào

Bước 6: Quá trình thêm các dNTP được tiến hành tuần tự. Lưu ý deoxyadenosine alfa-thio triphosphate (dATPαS) được sử dụng thay thế cho deoxyadenosine triphosphate (dATP) có có hoạt tính với DNA polymerase, nhưng không phải được nhận biết bởi luciferase. Khi quá trình này tiếp tục, các sợi DNA bổ sung được kéo dài và trình tự nucleotide được xác định từ các đỉnh tín hiệu trong phổ Pyrogram.
3. Tóm tắt điểm khác biệt giữa Pyrosequencing và Sanger Sequencing
Trình tự Sanger và Pyrosequencing là hai phương pháp lập trình DNA được sử dụng trong sinh học phân tử. Trình tự Sanger cấu trúc trình tự của các nucleotide theo trình tự bằng cách chấm dứt sự kéo dài chuỗi, trong khi pyrosequencing xây dựng thứ tự chính xác của các nucleotide theo trình tự bằng cách kết hợp nucleotide và phát hiện ra sự phóng thích của pyrophosphates. Vì vậy, sự khác biệt chính giữa trình tự Sanger và Pyrosequencing là giải trình tự Sanger làm việc theo trình tự bằng cách chấm dứt chuỗi, trong khi pyrosequencing làm việc theo trình tự bằng tổng hợp
Sản phẩm thương mại phổ biến đại diện cho phương pháp Pyrosequencing có nhà sản xuất Qiagen với các sản phẩm Pyromark Q24, Pyromark Q48 AutoPrep, Pyromark Q96. Roche cũng có 1 thiết bị giải trình tự thế hệ mới 454 Sequencing System dựa trên công nghệ Pyrosequencing (đã ngừng sản xuất).
Sản phẩm thương mại đại diện cho phương pháp Sanger Sequencing có Thermo Fisher Scientific (thương hiệu cũ là Apply Biosystem Inc) ngoài ra còn Beckman Coulter tuy nhiên hiện nay ít phổ biến ở thị trường Việt Nam do có nhiều điểm chưa đáp ứng được nhu cầu ứng dụng
Bảng so sánh
| Đặc điểm so sánh |
Pyrosequencing |
Sanger sequencing |
| Sản phẩm thương mại |
Pyromak Q24,
Pyromark Q48 AutoPrep,
Pyromark Q96
|
3500/3500XL Genetic Analyzer;
CQ 8000 Beckman Coulter
|
| Nguyên lý |
Giải trình tự trong quá trình tổng hợp (sequencing by Synthesis) bằng cách phát hiện PPi giải phóng khi 1 nu gẵn vào mạch khi đang tổng hợp
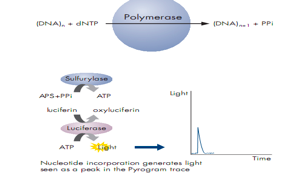
|
Tổng hợp các chuỗi hơn kém nhau 1 nucleotid sau đó điện di trên máy điện di mao quản (ABI hoặc Becman Coulter)
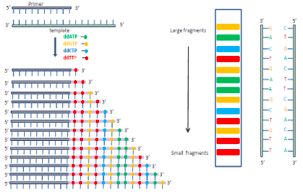
|
| Chuẩn bị mẫu |
Chỉ đưa sản phẩm PCR đã tinh sạch vào tinh sạch và đưa lên máy giải trình tự có ngay kết quả theo thời gian thực hoặc chỉ đưa Sản phẩm PCR lên máy (với một số dòng máy
|
Sản phẩm PCR sau tinh sạch cần chạy phảy PCR vòng 2, tinh sạch sau đó điện di trên máy giải trình tự |
| Công suất |
24 mẫu hoặc 96 mẫu/ 1 run |
8 mẫu hoặc 24 mẫu/1 run |
| Độ nhạy |
<2% trình tự đột biến và >98% Wt |
> 25% trình tự đột biến |
| Ứng dụng |
Phát hiện các đột biến (detection Mutation), định danh vi khuẩn, virus, đột biến kháng thuốc, độ nhạy cao khi nghiên cứu SNP, Định lượng Methylation |
Phát hiện đột biến đã biết hoặc tìm đột biến mới (Find Mutation), định danh vi khuẩn, virus, phân tích đoạn (VD STR - Huyết thống, Florescent PCR...)
|
| Kit thương mại |
Có các kit xét nghiệm ung thư: BRAS, KRAS, EGFR, NRAS… đạt tiêu chuẩn CE-IVD
|
Kit xét nghiệm cho huyết thống; QF-PCR; kit cho bệnh di truyền,
|
| Chức năng định lương allel |
Có |
Không |
| Định lượng đột biến |
Có |
Không |
| Phân tích STR cho huyết thống |
Không có kit
|
Là hệ thống duy nhất cho kit huyết thống dựa trên phân tích STR |
| Tiêu chuẩn |
Có kit và thiết bị đạt tiêu chuẩn cho chẩn đoán CE-IVD cho ung thư |
Có máy cho cho chẩn đoán, không có kit ung thư cho CE-IVD |
| Trình tự đọc ngắn có thể đọc được |
10bp |
>100 bp |
| Trình tự dài nhất có thể đọc |
<200 bp |
lên đến 900 bp |
| Vật tư tiêu hao thương mại |
Chạy ít mẫu không bị tốn chi phí hóa chất tiêu hao cho 24 mẫu.
|
Chạy 1 mẫu cũng tốn hóa chất và vật tư tiêu hao cho 8 mẫu (Với loại 8 mao quản) hoặc 24 mẫu (với loại 24 mao quản
|
| Quy trình thực hiện với thiết bị thương mại |
Đơn giản, không yêu cầu hoá chất tinh sản SP PCR. Có model tự động tinh sạch sản phẩm PCR cho giải trình tự tích hợp trong máy
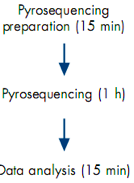
|
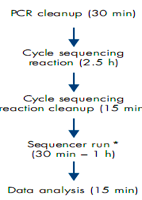
Nhiều bước, chi phí cao, mỗi bước đều yêu cầu sản phẩm phải được tinh sạch
|
Tài liệu tham khảo
- https://vi.esdifferent.com/difference-between-sanger-sequencing-and-pyrosequencing
- http://www.vsmmb.com/data/upload_file/File/PCR%20book%201/PCR_sequencing.pdf
- https://www.qiagen.com/us/resources/technologies/pyrosequencing-resource-center/technology-overview/